Implante auditivo de tronco cerebral en niños
Introducción
Candidatos al Implante
Historia
Resultados
Conclusiones
Bibliografía
Autores:
Prof. Dr. Vicente Guillermo Diamante
Lic. Norma Pallares
El Implante Auditivo del Tronco Cerebral (IATC) se usa desde 1979 para reestablecer la audición en pacientes con Neurofibromatosis tipo II (NF2) con sordera profunda bilateral en el momento de la remoción tumoral. Hace 5 años, se comienza a efectuar en adultos y niños con imposibilidad de realizarse un Implante Coclear (IC) por otras causas que no sean NF2. Los resultados auditivos obtenidos por el Dr. Vicente Diamante, primer autor en realizarlos en América, son mejores a los obtenidos con los IATC posterior a la remoción tumoral. Objetivo: Mostrar los resultados obtenidos mediante el uso del IATC en niños con imposibilidad de recibir un IC, con hipoacusia no asociada a NF2. Tipo de estudio: presentación de casos. Materiales y métodos: se muestran los resultados obtenidos en los dos primeros casos en América en niños (2 y 10 años respectivamente) a los que se les colocó un Implante Auditivo de Tronco Cerebral. Resultados: Se logró una ganancia en 30 a 40 db en las audiometrías posteriores a la activación, lograron detectar el Test de Ling en su totalidad, con buena y rápida respuesta al nombre. Conclusiones: Los estudios presentados demuestran que se obtienen resultados significativamente mejores, que en los pacientes implantados con NF-2. Colletti y colaboradores obtuvieron con el IATC en casos no tumorales, un promedio de reconocimiento de oraciones en forma sólo auditiva, sin lectura labial del 63%. En casos tumorales el promedio es de 12,2%. De acuerdo con estos resultados los casos no tumorales son considerados ideales para la colocación de un IATC porque la anatomía está intacta. El impacto de este tipo de implantes en la vida de lo pacientes ha resultado muy positivo.
Since 1979, the Brainstem Auditory Implant (BAI) has been used to restore the audition in patients with severe bilateral sensorineural HL and Neurofibromatosis type 2 (NF2). Five years ago it started to be used in adults and childrens without NF2 that could not undergo the use of a Cochlear Implant (CI). The results auditory obtained by Dr. Vicente Diamante, the first one to do them in America, are better than the ones obtained with the BAI in patients with NF2 after the tumor removal. Objectives: Show the results of the use of BAI en childrens that can not use CI with neurisensorial HL not related to NF2. Design of the study: Case report. Material and methods: we present the first results in America in two kids (2 y 10 years) that have a BAI. Results: Hearing improve between 30-40db in the audiometric controls posterior to dispositive activation, they could detect the whole Ling Test and have a good and fast reaction to calling their names. Conclusions: This cases prove that the results obtained are better that the ones in patients with NF2. Colletti et al. obtained in cases not tumoral with BAI recognition of oral sentences, without lips lecture of 63% , and in tumoral cases of 12.2%. According to this, cases that are nor tumoral are the best ones for the use of BAI because their anatomy is intact. The impact of this dispositives en patients of life is positive.
Key words: Brainstem Auditory Implant, cochlear implant, agenesis cochlea.
C.I.C Profesor Vicente Diamante, Pasteur 740, Buenos Aires, Argentina.
Introducción
La pérdida auditiva bilateral severa a profunda, es aceptada como una de las causas más comunes de discapacidad en el ser humano; según diferentes reportes entre el 1 y 3/1000 nacidos vivos presentan hipoacusia severa profunda por debajo de los 2 años de vida. Tienen dificultad de oír cualquier estímulo que provenga del mundo exterior. Esta situación es dramática en los niños, pero crítica en los adultos. Si la hipoacusia se produce en estadíos tempranos (periodo prelingual) producirá graves consecuencias en el desarrollo del lenguaje con dificultades para aprender, participar, comprender e interactuar con el mundo que los rodea.
La pérdida sensorial es producida en el 98% de los casos por alteraciones cocleares, y el resto de ellas por alteraciones del nervio auditivo o de la vía auditiva. Se debe intentar el diagnóstico y tratamiento o internación temprana, la cual mejorará el pronóstico. El mismo debe realizarse según el grado de pérdida auditiva; cuando es leve o moderada, el audífono bilateral es la mejor opción; cuando la falla está en la cóclea en ausencia de patología del nervio auditivo y se acompaña de sordera profunda a severa, la indicación es de implante coclear (IC). Decenas de miles de pacientes se benefician con el uso del IC uni o bilateral.
La aparición de los IC para la rehabilitación de pacientes con hipoacusias profundas o totales, bilaterales, sensoriales significa el comienzo de la utilización de las señales eléctricas para proveer audiabilidad en esos casos donde el uso de audífonos no lo lograba. La condición es una cóclea lesionada y un nervio funcionante.
De manera tal que los pacientes que por diversas causas tenían una lesión del nervio auditivo entre el ganglio espiral y los núcleos cocleares del tronco cerebral no podían beneficiarse de una prótesis coclear y quedaban aislados en un mundo de silencio. En esos casos donde el nervio está lesionado no es posible la realización de un implante coclear y podría ser beneficiosa la utilización de un Implante Auditivo del Tronco Cerebral (IATC), que directamente estimula los núcleos cocleares (NC). Estos dispositivos están diseñados hasta ahora, para estimular los NC en su superficie y también en profundidad, con la posibilidad de proporcionar sensaciones auditivas a individuos con lesiones del nervio auditivo.
Actualmente, más de 500 pacientes con Neurofibromatosis tipo II (NF-2) con tumores en ambos oídos que han sido implantados con IATC, han recibido en su mayoría (85%) información auditiva con la que mejoran sus habilidades comunicativas, escuchan ruidos ambientales, tienen información auditiva del habla (especialmente suprasegmental: acento, duración, ritmo) lo que los ayuda con la lectura labial (LL). Un porcentaje limitado, es capaz de reconocer el habla en formato abierto sin la ayuda de la LL. Esta realización general es considerada semejante a la obtenida en pacientes con IC monocanal. El IC multicanal en cambio, ha posibilitado a pacientes adultos postlinguales llegar a entender el habla telefónica.
La FDA permite implantes auditivos de tronco cerebral
solamente para pacientes con NF mayores de 12 años.
(1)
Para quienes presentan alteraciones intrínsecas de la cóclea que impide el IC o neuropatías de otras etiologías no está autorizada la colocación de ABI.
Hace 5 años, el primer autor en el mundo en ampliar las indicaciones del ABI en niños y adultos no tumorales, fue el Profesor Vittorio Colleti, de Verona, Italia. Si solo se realiza ABI en aquellos pacientes que sufren de sordera por NF-2, siguiendo estrictamente las indicaciones de la FDA, se subestima la posibilidad de recuperación de los otros casos, lo que conlleva a que un número grande de individuos no puedan beneficiarse con un ABI, según el criterio de Colletti. A partir de ese concepto él comenzó a aplicar el uso de ABI en casos no tumorales y en niños. (2, 3, 4, 5, 6)
En la actualidad se está utilizando el IATC en una serie de pacientes, niños y adultos, en casos no tumorales: con aplasia o hipoplasia del nervio coclear, con grandes malformaciones cocleares o agenesia de cóclea, con fractura de base de cráneo, con avulsión del VIII par, con severa osificación coclear. La causa de esa gran diferencia de realización observada entre el IC y el IATC está en estudio, donde en general los dispositivos son semejantes pero la gran diferencia radica en el lugar de estimulación.
Ha sido observado por el Prof. Colletti, que en adultos pos-linguales en los casos no tumorales detallados con anterioridad, el IATC brinda resultados semejantes a los obtenidos con un IC incluyendo el uso del teléfono. Los resultados en niños sordos congénitos en los que el IC no se puede realizar, también son positivos.
El implante auditivo de tronco cerebral es hasta el momento la intervención más desafiante en el gran capítulo de la rehabilitación auditiva. En casos especiales, constituye la única posibilidad de realizar un by pass de la cóclea y el nervio auditivo, estimulando directamente la 2º neurona de la vía auditiva, estableciendo la conexión entre el mundo sonoro y el componente central de la vía auditiva, que hasta ese momento había estado totalmente privada de estimulación. (Ver Gráfico 1) (7)
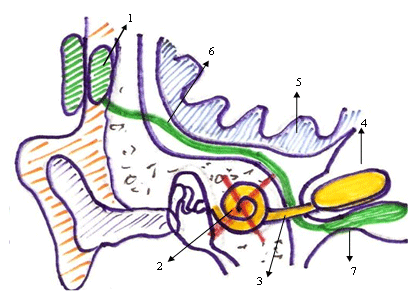
Gráfico 1: 1) receptor interno del implante, 2) cóclea, 3) Nervio auditivo, 4) Núcleos Auditivos del bulbo, 5) Corteza, 6) Electrodo, 7) contacto entre electrodo y núcleo.
La experiencia en la remoción de tumores en casos de NF-2 simultáneamente a la colocación de ABI, durante 25 años, permite tener la certeza que la colocación del ABI no se asocia a un aumento de la morbilidad ni de las complicaciones postoperatorias. El hecho de saber que la estimulación directa de los núcleos del piso del IV ventrículo no producen alteraciones anatómicas ni funcionales de la vía auditiva, y de las área vecinas, hace posible la idea de realizar el implante de tronco en niños desde muy temprana edad.
El 5 de marzo del 2007, el Prof. Diamante con la presencia del Prof. Colletti, relizaron en Buenos Aires, la primera cirugía para la colocación de un IATC en una niña de 2 años con agenesia de cóclea y de nervio. Este es el primer caso en toda América.
El 18 de abril del 2007, se operó otra niña de 10 años con agenesia de ambos nervios auditivos.
El implante auditivo de tronco cerebral por definición, es un dispositivo que promueve sensaciones auditivas a pacientes con sordera total bilateral, por alteración o agenesia del axón de la 1º neurona de la vía auditiva o de la cóclea estimulando directamente los núcleos ventral y dorsal de la misma.
El equipo consiste en una versión modificada del IC Nucleus, con un electrodo que puede ser introducido en el receso lateral del bulbo.
Desde el punto de vista quirúrgico, se puede
acceder al área en cuestión mediante el
abordaje translaberíntico o suboccipital. Los
elementos de reparo para encontrar el Foramen de Luschka,
que es la parte más lateral del receso lateral
son: VII, VIII, IX pares craneales, que se observan
sin dificultad, una vez que se ha reclinado el flóculo
cerebeloso. (Ver Gráfico 2) A través de
dicho foramen emergen los plexos coroideos, que son
el punto de referencia anatómico fundamental.
Una vez introducido el electrodo en el receso lateral,
se debe realizar un BERA eléctrico para poder
determinar si hay respuesta auditiva. (Ver Figura 1)
Lo que indica que el electrodo está colocado
sobre los núcleos auditivos. (Ver Figuras 2-3-4-5-6-7-8)
(8)
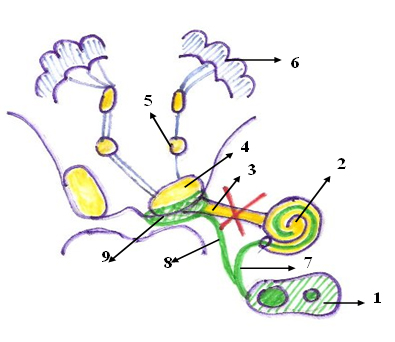
Gráfico 2: 1) Receptor interno del implante, 2) cóclea, 3) Nervio auditivo, 4) Núcleos auditivos del bulbo, 5) Vía Auditiva, 6) Corteza cerebral auditiva, 7) Electrodo en cóclea, 8) Electrodo a los Núcleos y 9) Conectado entre los núcleos.
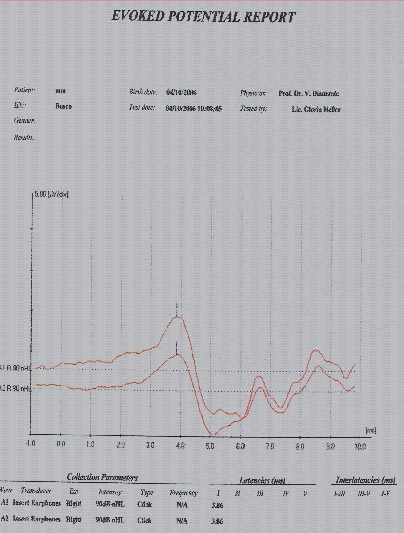
Fig.1: Registro del BERA eléctrico intraoperatorio en onda 3.
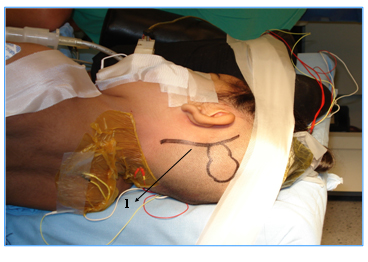
Fig. 2: Posición quirúrgica, 1) marcado de las incisiones y del receptor interno.
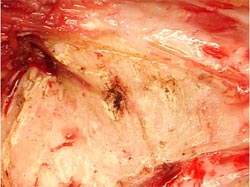
Fig. 3:
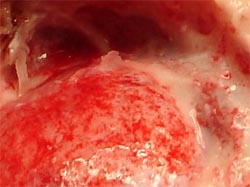
Fig. 4:
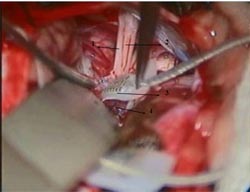
Fig. 5: 1) Nervio acústico, 2) Nervio glosofaríngeo,
3) Plexos Coroideos,
4) Electrodo.
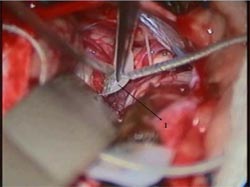
Fig. 6: 1) Electrodo penetrando por el forámen
de Lushka al receso lateral del bulbo.
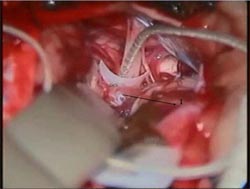
Fig. 7: 1) Posición definitiva del electrodo
sostenido con músculo.
Candidatos al Implante
Según la FDA los candidatos al implante de tronco deben cumplir los siguientes criterios: (9, 10)
1-
Diagnóstico de NFII
2- Necesidad de remoción tumoral
3- Ser mayor de 12 años
4- Expectativas razonables
5- Compromiso de seguimiento
Las nuevas indicaciones del implante de tronco en casos no tumorales para niños y adultos son: (11)
1-
Agenesia de cóclea
2- Agenesia de nervio auditivo
3- Grandes malformaciones de oído interno
4- Estallido traumático de ambas cócleas
5- Sección de ambos nervios auditivos
6- Cócleas osificadas post meningitis con malos
resultados con IC.
7- Otoespongiosis masiva bilateral, otoesclerosis, osteogénesis
imperfecta o enfermedad de Paget que hayan obtenido
pobres resultados con IC.
8- Neuronopatías auditivas que no respondieron
a este dispositivo.
(Ver Figuras 9-10-11-12 y 13)
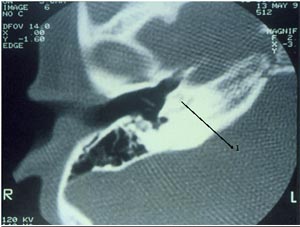
Fig. 9: 1) Cóclea totalmente osificada.
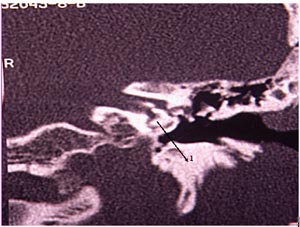
Fig. 10: 1) Rotura múltiple de cóclea.
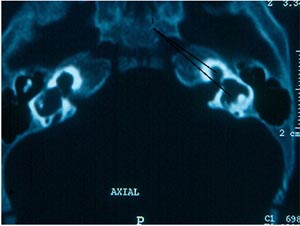
Fig. 11: 1) Gran malformación de cóclea
y laberinto posterior con amplia
Comunicación al espacio subaracnoideo.
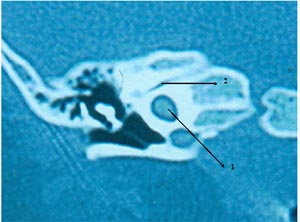
Fig. 12: 1) Cisterna coclear, 2) CAI muy fino para el
paso del N. Facial con
Agenesia del N. Auditivo.
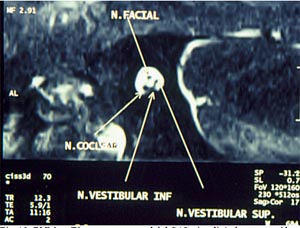
Fig. 13: RNM en T2: corte transversal del CAI, visualizándose
contenido
Líquido y los nervios normales.
Historia
El primer IATC fue desarrollado en el House Ear Institute y fue realizado en 1979 por los doctores William House y William Hitselberger. (12) En ese momento el dispositivo utilizado fue una prótesis monocanal con un electrodo bolita y un sistema de transmisión percutáneo basado en el sistema 3M-House de implantes cocleares. El paciente tenía sordera bilateral, secundaria a la extracción de tumores bilaterales del nervio auditivo debido a NF-2. Luego de esta primera experiencia, los investigadores del Instituto House desarrollaron un dispositivo más adecuado para ser colocado en el receso lateral, que consistía en dos electrodos de platino montados en una pieza de dacron rectangular, diseñada para promover la integración fibrosa. Luego, 25 pacientes fueron implantados con este de 2 electrodos y luego con otro similar de 3 electrodos. Estas partes internas se conectaban al procesador 3M-House.
El diseño de los electrodos han ido variando desde las primeras tentativas de estimular eléctricamente los NC y en consecuencia los resultados han mejorado y se ha logrado una mayor estabilización del dispositivo.
En 1989 se comenzó a desarrollar una nueva generación de IATC, los implantes multicanales, basados en el sistema Nucleus 22 de Cochlear, esto ocurrió por un trabajo conjunto entre el House Ear Institute, Cochlear Corporation y el Huntington Medical Research Institute.
En 1992, fue implantado el primer paciente con este dispositivo de 8 electrodos de superficie. Esta prótesis multicanal ha sido desarrollada, basándose en el implante coclear Nucleus 22. La placa de electrodos se coloca sobre la superficie de los NC, en el receso lateral del cuarto ventrículo en el momento de la extracción translaberíntica del tumor. La estimulación se realiza a través de un sistema transcutáneo, pudiendo utilizarse una variedad de estrategias de comunicación y modos de estimulación, dependiendo de las respuestas individuales frente a la estimulación eléctrica. En la mayoría de los casos, ha sido posible utilizar múltiples electrodos en los mapas de calibración, con mayores posibilidades de éxito en el manejo de las sensaciones no auditivas, frecuentes en este tipo de pacientes.
En 1998 el “Centro de Implantes Cocleares Profesor Diamante”, fue el primer grupo en Sur América autorizado para la realización del IATC.
Posteriormente, surgió el IATC Nucleus 24 con 21 electrodos en una placa y más recientemente, fruto de intensos trabajos de investigación se está utilizando el electrodo de inserción profunda, con experiencia reciente y limitada en seres humanos.
Otras fábricas tienen prototipos similares de IATC, como es el caso de Medel, Clarion y Digisonic. (13)
En la actualidad, se han presentado tres casos de pacientes con IATC colocado para estimular eléctricamente el colículo inferior, los resultados son promisorios, aunque los NC continúan siendo el lugar de óptima elección para la colocación de un IATC.
La
indicación del IATC en niños está
referida a:
• Imposibilidad de realizar o fracaso con un IC.
• Ausencia de déficits neurológicos
que impidan la habilitación auditiva.
• Familia motivada y ambiente social adecuado.
• Experiencia en cirugía de fosa posterior
por parte del equipo quirúrgico.
• Experiencia en el tema de habilitación
auditiva por parte del resto del equipo.
• Posibilidad d prolonga da e intensa habilitación.
Resultados
El ABI permite la percepción de sonidos ambientales, monosílabos o bisílabos en formato cerrado. Un porcentaje reducido de pacientes llegan a la percepción en formato abierto. Todos ellos tienen una mejoría fundamental en la lectura labial. Vittorio Colletti, marca una diferencia significativa en relación a los resultados obtenidos entre los pacientes con resección tumoral y los pacientes no tumorales. En los adultos no tumorales, el reconocimiento de palabras y monosílabos en formato cerrado al año, es del 86% y en los casos tumorales es del 24%. Con respecto a la percepción de oraciones sin lectura labial, en casos no tumorales es del 66% al año y en los tumorales es del 20%. Los niños prelinguales perciben los bisílabos al año en un 30 % en formato cerrado, y el 25 % llega a la percepción de oraciones en formato abierto. De esta manera, si nos ajustamos a las indicaciones de la F.D.A. no estaríamos ayudando a una serie de pacientes con patología no tumoral que puede ser beneficada con el uso de un ABI. Los resultados favorables obtenidos en los pacientes no tumorales en relación a los tumorales, se dan debido a que en los últimos, el tumor distorsiona la anatomía de los núcleos auditivos, comprimiendo y desplazando al tronco cerebral, dificultando a su vez la salida de LCR del receso lateral del IV ventrículo lo que produce edema, fibrosis e isquemia de las estructuras vecinas. Además, durante la cirugía de remoción tumoral se pueden producir, mediante la tracción y microcoagulación, interferencias en la vascularización de los núcleos. Según el profesor Colleti, las diferencias pueden ser observadas durante la cirugía mediante las respuestas telemétricas, ya que en los casos tumorales se observan umbrales más altos que aquellos obtenidos en pacientes sin tumores, así como también existe un mayor número de electrodos activos con umbrales más estables en pacientes no tumorales.
Colletti,
ha obtenido resultados significativos, en los casos
de niños que presentaban grandes malformaciones
cocleares y de osificaciones cocleares con falla en
los resultados del IC que recibieron posteriormente
un ABI.
Un aspecto fundamental al momento de realizar la intervención
en los niños, es el tener la seguridad de la
presencia de los núcleos cocleares en ausencia
del nervio. Su presencia se puede verificar mediante
TAC y RMN en base al nivel de los mismos asociados a
un IV ventrículo y tronco cerebral normales.
Embriológicamente parecería que el desarrollo de la cóclea es independiente del nervio, y que la presencia del mismo no provee ningún efecto trófico sobre los núcleos. Se podría presumir que los núcleos no necesitan para su desarrollo ser estimulados por la vía aferente.
Sin estímulos aferentes los núcleos no deben poseer arquitectura tonotópica y de ser así, sería beneficioso en los niños, porque la tonotopía se iría produciendo en la medida que los núcleos sean estimulados eléctricamente por los electrodos de distintas frecuencias colocadas en su contacto, según Colletti.
Los resultados a los 7 días de nuestros dos casos fueron:
1)
Luciana 3años
AT: entre 30 y 40 db
Detecta todo el Test de Ling (a-u-i-m-sh-s)
Comienza a identificar diferencias suprasegmentales
(básicamente duración)
Muy buena y rápida respuesta al nombre
Aceptación total de la estimulación
Por las mañanas solicita que le coloquen el implante
2)
Candelaria 10 años
AT: entre 35 y 40db
Detecta todo el Test de Ling (a-u-i-m-sh-s)
Identifica diferencias espectrales (estaría en
una categoría 2)
Comienza a identificar palabras de igual duración
por diferencias espectrales (categoría 3)
Responde al nombre con facilidad
Disfruta escuchar todos los ruidos ambientales (como
agua, música)
No grita al hablar y no arrastra más los pies
al caminar
Fig. 14: Dibujos de Candelaria con los sonidos que escucha.

Fig. 15: Dibujos de Candelaria con los sonidos que escucha

Fig. 16: Dibujos de Candelaria con los sonidos que escucha.
El IATC ha sido considerado hasta hace pocos años sólo en los pacientes con NF-2 en especial cuando se realiza la cirugía para la extracción del neurinoma. Actualmente, se está considerando en adultos y niños la utilización de este tipo de prótesis en pacientes con las causas no tumorales ya detalladas.
Los estudios presentados demuestran que estos, obtienen resultados significativamente mejores que los pacientes implantados por NF-2. Colletti y colaboradores obtuvieron con el IATC en casos no tumorales, un promedio de reconocimiento de oraciones en forma sólo auditiva, sin LL, en torno al 63%. En casos tumorales el promedio es de 12,2%. De acuerdo con estos resultados los casos no tumorales son considerados ideales para la colocación de un IATC porque la anatomía está intacta.
El grupo de IATC consiste de profesionales de muchas disciplinas: otología, neuro-otología, audiología, elctrodisiología, neurocirugía, neurología, psicología, participando también con frecuencia oftalmólogos y genetistas.
El impacto de este tipo de implantes en la vida de esos pacientes ha resultado muy positivo.
Los resultados observados son interesantes y aumentan nuestro conocimiento sobre las potencialidades del sistema auditivo central frente al estímulo eléctrico y las posibilidades de realización auditiva con la estimulación eléctrica en la superficie de los núcleos cocleares del tronco cerebral, haciendo un by-pass de la cóclea y el nervio.
1. Otto SR, Brackman DE, Hitselberger WE. (2004). Auditory brainstem implantation in 12-to 18- Years Olds. Arch Otolaryngol Head and Neck Surg 130:656-659.
2. Colletti V, Fiorino F, Carner M, Sacchetto L, Miorelli V, Orsi A. (2002). Auditory brainstem implantation: the University of Verona experience. Otolaryngol Head and Neck Surg 127:84-96.
3. Colletti V, Fiorino F, Carner M, et al. (2002). Hearing
restoration with auditory
brainstem implant in three children with cochlear nerve
aplasia. Otol Neurotol
23:682-693.
4.
Colletti V, Fiorino F, Carner M, Miorelli V, Guida M,
Colletti L. (2004).
Auditory brainstem implant as a salvage treatment after
unsuccessful cochlear
implantation. Otol Neurotol 25:485-496.
5. Colletti V, Carner M, Miorelli V, Guida M, Colletti L, Fiorino F. (2004). Cochlear implant failure: Is an auditory brainstem implant the answer? Acta Otolaryngol 124:353-357.
6. Colletti V, Carner M, Miorelli V, Guida M, Colletti L, Fiorino F. (2005). Auditory brainstem implant: new frontiers in adults and children. Otolaryngol Head and Neck Surg 133:126-138.
7. McEleven JT Jr, Hitselberger WE, House WF. (1987). Surgical accessibility of the cochlear nuclear complex in man: surgical landmarks. Otolaryngol Head and Neck Surg 96:135-140.
8. Terr Ll, Fayad J, Hitselberger WE, Z akhary R. (1990). Cochlear nucleus anatomy related to central electro auditory prosthesis implantation. Otolaryngol Head and Neck Surg 102:717-721
9. Laszig R, Sollmann WP, Marangos N. (1995). The restoration of hearing in Neurofibromatosis type 2. J Latyngol Otol 109:385-389.
10. Lenarz M, Matthies C, Lesinski-Schiedat A, et al. (2002). Auditory brainstem implant Part II: subjective assessment of functional outcome. Otol Neurotol 23:694-697.
11. Grayeli AB, Bouccara D, Kalamarides M, et al. (2003). Auditory brainstem implant in Bilateral and completely ossified cochleae. Otol Neurotol 24:79-82.